近日,Nature Communications在线发表了江南大学未来食品科学中心陈坚院士团队康振教授课题组的研究性论文“Regulating cellular metabolism and morphology to achieve high-yield synthesis of hyaluronan with controllable molecular weights”。江南大学2020级博士胡立涛为第一作者,康振教授为通讯作者,合作单位包括宜兴食品与生物技术研究院等。
透明质酸(HA)作为一种高价值糖胺聚糖,在医药、化妆品及生物材料等领域应用广泛,但其高效生物合成与分子量的精准控制仍是当前研究的核心难点。传统合成技术受限于I型透明质酸合酶(HAS)功能解析不足及细胞代谢-形态失衡的双重挑战:一方面,HAS的跨膜通道构象调控机制不明,导致HA链延伸与转运效率低下;另一方面,宿主细胞代谢通量分配不合理及高黏度发酵环境易引发细胞形态畸变与代谢停滞,严重制约产量与分子量可控性。
为了解决这一难题,研究团队通过解析HAS跨膜通道构象调控机制,构建了可实现HA完全分泌且分子量范围扩展至300-1400 kDa的突变体。首先,研究人员发现SzHAS因跨膜通道构象异常导致HA胞内积累及细胞形态畸变(图1)。为验证跨膜通道构象调控的关键性,研究人员替换SzHAS的TMH-1片段为SpHAS对应区域,突变体SzHASSpTMH-1恢复HA分泌能力(图2)。随后,研究人员系统性鉴定了跨膜通道TMH-1参与调控HA转运的关键氨基酸位点(图3),并整合有益突变以及系统性突变筛选SzHAS催化域中12个非保守位点获得最佳突变体(图4)。此外,研究人员采用对数生长期晚期启动子动态调控UDP-葡萄糖醛酸合成,协调细胞生长与HA高产(图5)。最后,研究人员通过适应性驯化策略提升菌株高黏度耐受性,最终在5 L发酵罐中实现中高分子量HA 45 g·L⁻¹的发酵水平,进一步结合水蛭源透明质酸酶消除HA荚膜层,实现低分子量HA产量高达105 g·L⁻¹(图6)。
上述工作得到了国家重点研发计划(2024YFF1106300)、国家自然科学基金(U24A20368)、江苏省合成生物学基础研究中心(BK20233003)、食品科学国家重点实验室研究计划(BK20233003)、无锡市产业创新研究院先导研究计划(XD24006)和江南大学食品科学与资源国家重点实验室研究计划(SKLF-ZZB-202418)的资助。
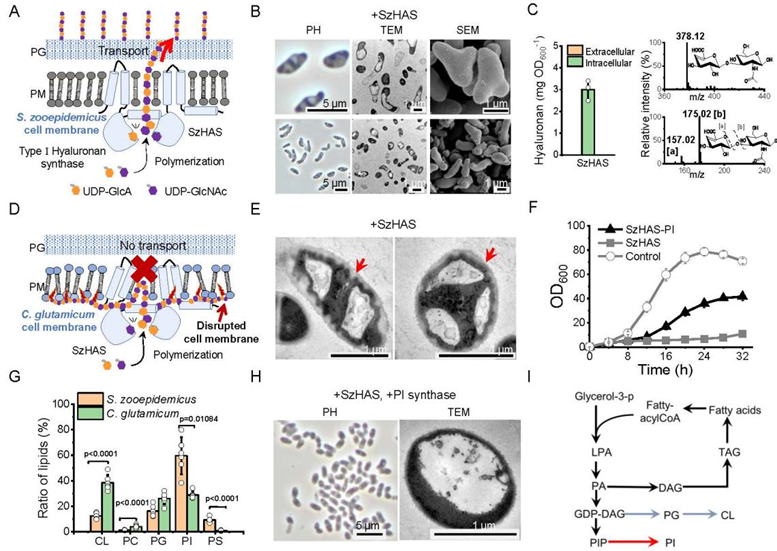
图1 SzHAS失去HA跨膜转运能力导致细胞质积累
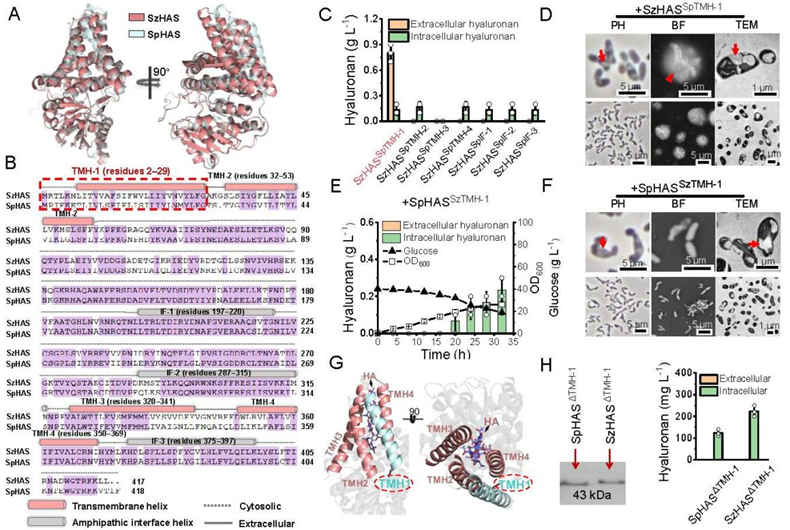
图2 SzHAS跨膜螺旋TMH-1功能鉴定
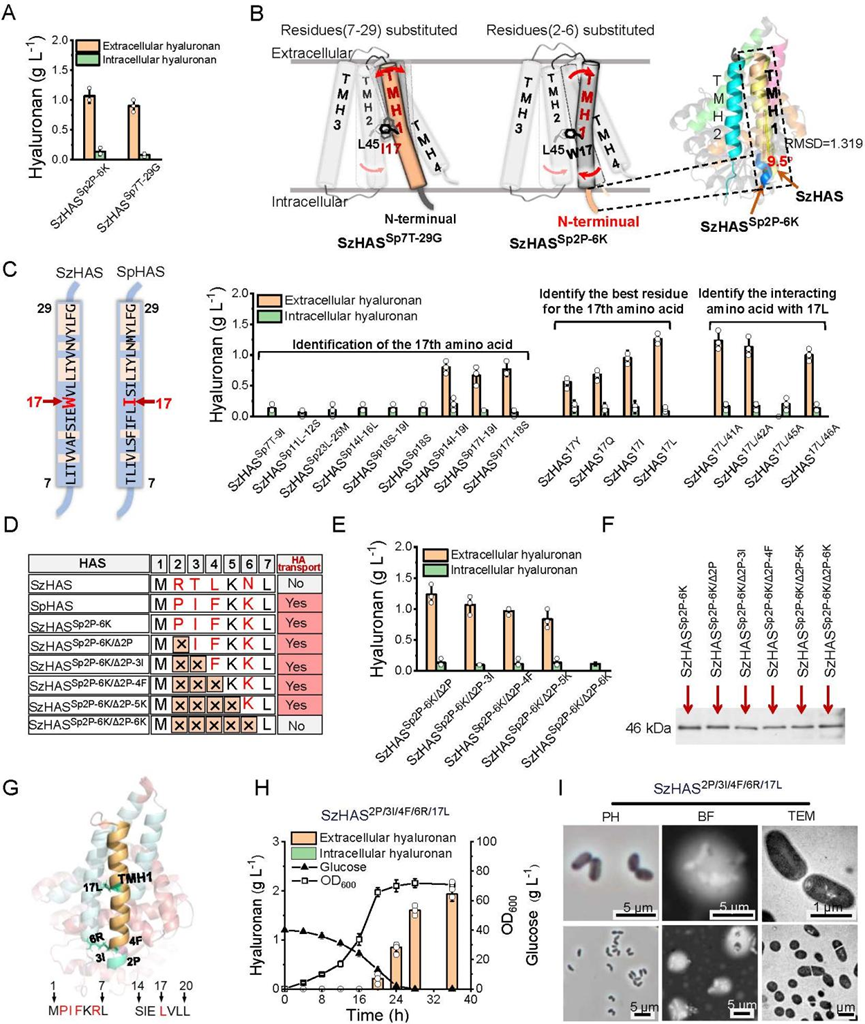
图3 SzHAS跨膜转运通道重构实现HA完全转运
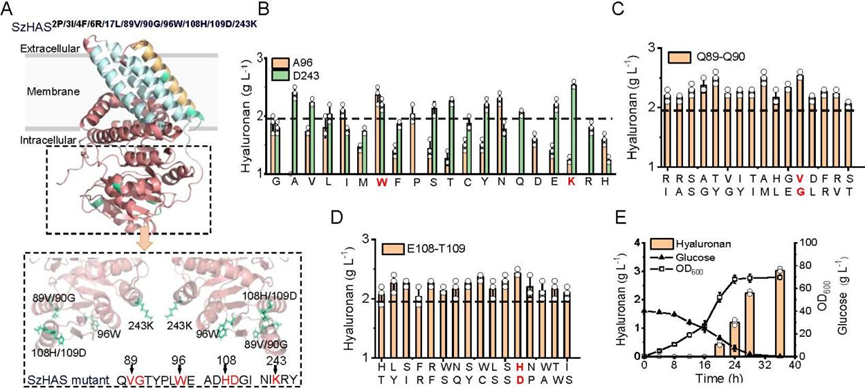
图4 SzHAS胞内催化结构域关键氨基酸位点鉴定与改造
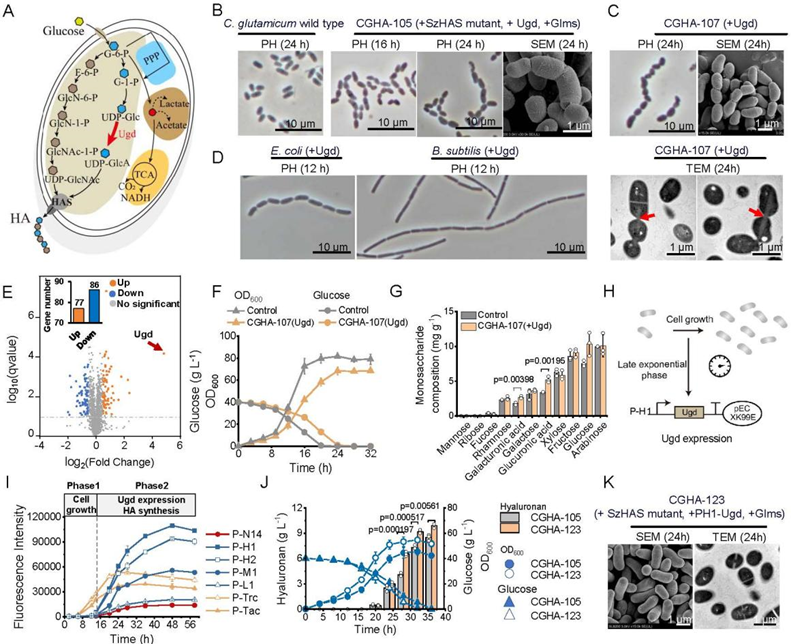
图5 构建对数生长期晚期启动子调控UDP-葡萄糖醛酸合成
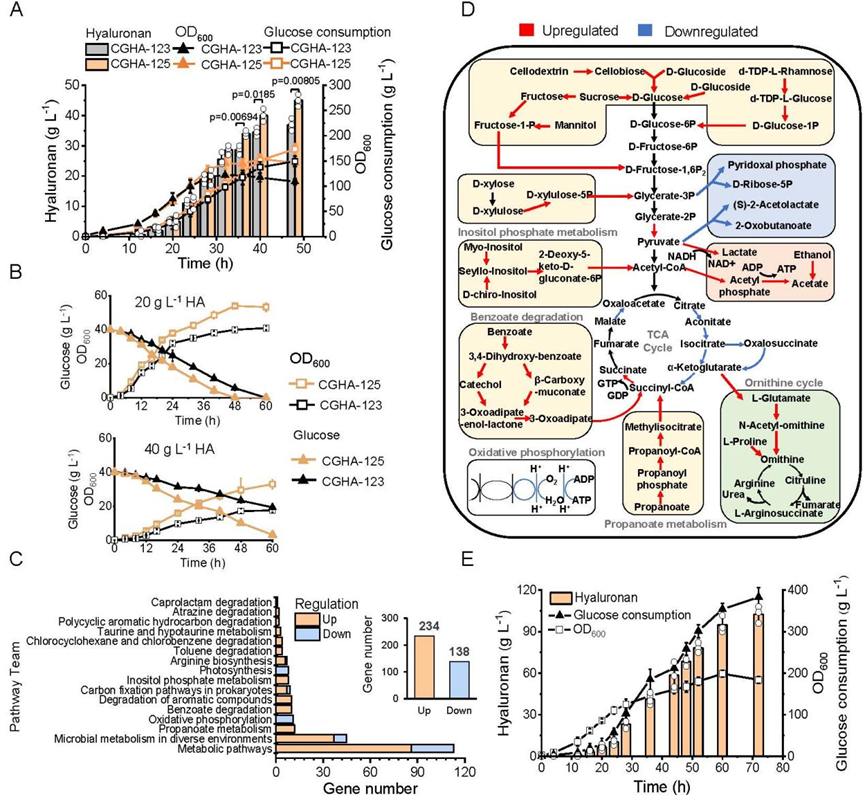
图6 适应性驯化提升菌株高浓度HA耐受性对HA合成的影响
